- Trang chủ
- Giới thiệu
- Giới thiệu chung
- Tổ chức bệnh viện
- Ban giám đốc
- Khối phòng ban
- Các khoa hệ nội
- Khoa Cấp cứu chống độc
- Khoa Truyền nhiễm
- Khoa Nội A - Lão học
- Khoa Nội tiết
- Khoa Tim mạch
- Khoa Y học cổ truyền
- Khoa Khám bệnh theo yêu cầu
- Khoa Điều trị theo yêu cầu
- Khoa Vật lý trị liệu - Phục hồi chức năng
- Khoa Nội tổng hợp
- Khoa Nhi
- Khoa Hồi sức tích cực
- Khoa Nội Thận - Tiết niệu - Cơ - Xương - Khớp
- Khoa Da liễu
- Khoa Khám bệnh
- Khoa Ung bướu - Y học hạt nhân
- Các khoa hệ ngoại
- Các khoa cận lâm sàng
- Các thành tích đạt được
- Danh bạ điện thoại
- Tin tức và sự kiện
- Đào tạo chỉ đạo tuyến
- Dịch vụ khám và điều trị
- Thông tin y dược
- Tư vấn giáo dục sức khỏe
- KQ Khảo Sát



FDA HOA KỲ PHÊ DUYỆT LIỆU PHÁP KẾT HỢP AVMAPKI FAKZYNJA CỦA VERASTEM ĐỂ ĐIỀU TRỊ BỆNH NHÂN MẮC UNG THƯ BUỒNG TRỨNG BIỂU MÔ THẤP TÁI PHÁT CÓ ĐỘT BIẾN KRAS
Ngày đăng: 14/05/2025 - Lượt xem: 397
Ngày đăng: 14/05/2025 - Lượt xem: 397
Ngày 8 tháng 5 năm 2025, Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) đã phê duyệt Avmapki Fakzynja Co-Pack (avutometinib và defactinib kết hợp) để điều trị ung thư buồng trứng biểu mô thấp tái phát có đột biến KRAS ở người lớn. Đây là liệu pháp đầu tiên được phê duyệt dành riêng cho loại ung thư hiếm gặp này.
Thông tin cơ bản:
- Tên thương mại: Avmapki Fakzynja Co-Pack
- Hoạt chất: avutometinib (ức chế MEK) và defactinib (ức chế FAK)
- Dạng bào chế: Viên nén.
- Chỉ định: Điều trị ung thư buồng trứng biểu mô thấp tái phát có đột biến KRAS sau liệu pháp hệ thống trước đó.
- Cơ chế tác dụng: Avutometinib ức chế enzym MEK, trong khi defactinib ức chế FAK, cả hai đều nhắm vào con đường tín hiệu KRAS, ngăn chặn sự phát triển và lan rộng của tế bào ung thư.
Liều lượng và cách dùng
- Liều ban đầu: Avutometinib: 3,2 mg uống hai lần mỗi ngày, defactinib: 200 mg uống hai lần mỗi ngày, trên dạ dày rỗng (ít nhất 1 giờ trước hoặc 2 giờ sau ăn).
- Lịch trình: Chu kỳ 28 ngày, lặp lại cho đến khi bệnh tiến triển hoặc không dung nạp.
- Điều chỉnh liều: Giảm liều nếu có độc tính cấp độ 3 hoặc 4, theo hướng dẫn của bác sĩ.
- Liều ở bệnh nhân suy gan hoặc suy thận: Không cần điều chỉnh, nhưng cần theo dõi chặt chẽ.
- Tương tác thuốc: Tránh dùng với chất ức chế CYP3A mạnh, có thể tăng độc tính.
Chống chỉ định và cảnh báo
- Chống chỉ định: Không dùng cho bệnh nhân có dị ứng với avutometinib, defactinib, hoặc các thành phần của thuốc.
- Cảnh báo:
+ Nguy cơ độc tính tim mạch, bao gồm kéo dài QTc và suy tim.
+ Tăng nguy cơ chảy máu, đặc biệt ở bệnh nhân dùng thuốc chống đông.
+ Có thể gây tổn thương gan, cần theo dõi chức năng gan định kỳ.
Tác dụng phụ
>10%: Mệt mỏi (15%), buồn nôn (12%), tiêu chảy (11%).
1-10%: Phát ban (8%), tăng enzym gan (5%), chảy máu (3%).
Sử dụng ở nhóm đặc biệt
- Phụ nữ mang thai: Dữ liệu hạn chế, khuyến cáo tránh sử dụng nếu không cần thiết.
- Phụ nữ cho con bú: Không khuyến cáo sử dụng, do nguy cơ tiềm ẩn cho trẻ.
- Trẻ em: An toàn và hiệu quả chưa được thiết lập.
Nghiên cứu lâm sàng
- Cơ sở phê duyệt: Dựa trên nghiên cứu lâm sàng giai đoạn 3, cho thấy tỷ lệ đáp ứng cao hơn so với placebo ở bệnh nhân ung thư buồng trứng biểu mô thấp tái phát có đột biến KRAS.
- Kết quả chính: Tỷ lệ đáp ứng toàn bộ (ORR) đạt 46%, thời gian sống không tiến triển (PFS) trung bình là 7,2 tháng.
Kết luận
Avmapki Fakzynja Co-Pack là một bước tiến quan trọng trong điều trị ung thư buồng trứng biểu mô thấp tái phát có đột biến KRAS. Với cơ chế tác dụng nhắm vào con đường tín hiệu KRAS và hồ sơ an toàn tương đối tốt, thuốc mang lại hy vọng cho bệnh nhân và là một chủ đề quan trọng trong nghiên cứu dược lâm sàng hiện đại.
Nguồn
1. FDA
2. Drugs.com

Hình ảnh hoạt động nổi bật

Video Bệnh viện

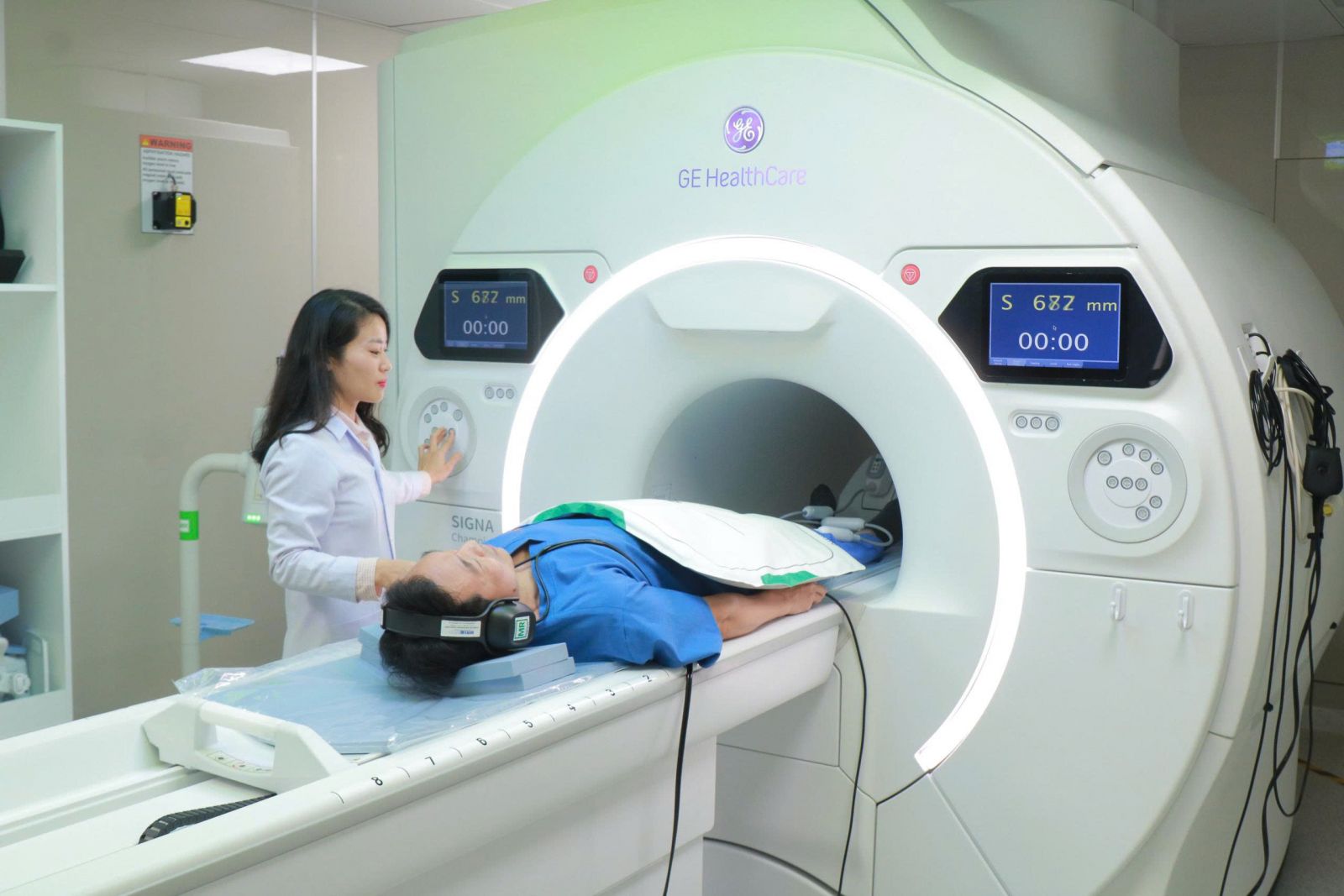
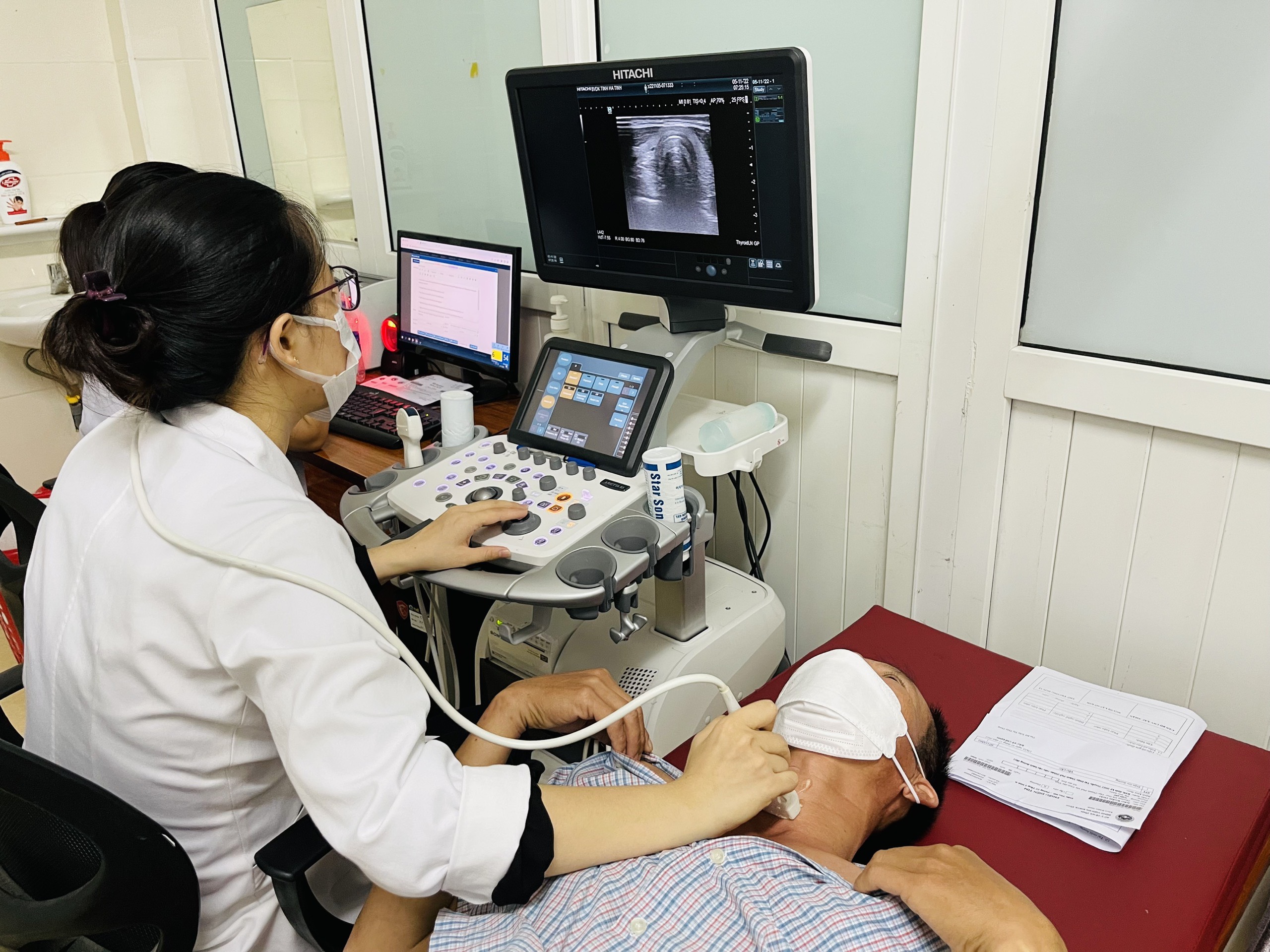
Trang thiết bị hiện đại

Các dịch vụ kỹ thuật cao

Dịch vụ khám, điều trị theo yêu cầu

Liên hệ / Gửi câu hỏi

Thống kê truy cập
Online: 31
Tổng lượt truy cập: 32205695
Hôm nay: 4910







 Phẫu thuật thay khớp vai nhân tạo
Phẫu thuật thay khớp vai nhân tạo Thay máu sơ sinh do bất đồng nhóm máu
Thay máu sơ sinh do bất đồng nhóm máu Tán sỏi niệu quản ngược dòng Laser
Tán sỏi niệu quản ngược dòng Laser Phẫu thuật Cột sống
Phẫu thuật Cột sống
















